dal-Vessel: Vasculaire effecten en veiligheid CETP inhibitie
Literatuur - Luscher TF:et al, Eur Heart J. 2012 Feb 16dal-VESSEL: Werkzaamheid en veiligheid van dalcetrapib bij patiënten met of met risico op coronaire hartziekten – de dal-VESSEL studie
Lüscher TF, Taddei S, Kaski JC, Jukema JW, Kallend D, Münzel T, Kastelein JJ, Deanfield JE; on behalf of the dal-VESSEL Investigators.
Eur Heart J. 2012 Feb 16.
Achtergrond
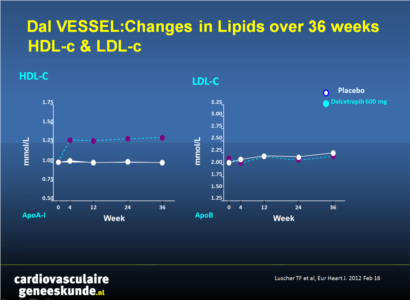
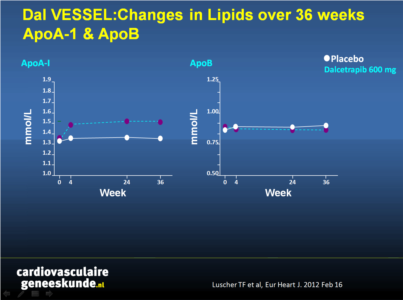
Dit is een fase 2 multi-center studie ter evaluatie van de haalbaarheid om flow- gemedieerde dilatatie en beoordeling van risico markers te gebruiken. De onderzoekers analyseerden een nieuwe verbinding (dalcetrapib), die cholesterol ester transfer protein (CETP) vermindert met ongeveer 49% en het HDL-cholesterol verhoogt met ongeveer 31%.
Met behulp van gevalideerde technieken om flow-gemedieerde dilatatie in de slagader te beoordelen, onderzochten ze het effect van dalcetrapib op de NO-afhankelijk endotheelfunctie, bloeddruk en markers van ontsteking en oxidatieve stress.
De resultaten van deze studie werden gepresenteerd op het ESC 2011 [zie vorige posting - link] en zijn nu in EHJ gepubliceerd.
Redactioneel commentaar [1]
De auteurs concludeerden dat dalcetrapib geen enkele nadelige effecten had op de endotheelfunctie of de arteriële bloeddruk. Met betrekking tot de bekende gunstige effecten van HDL op endotheelfunctie zoals gemeten door endotheel-afhankelijke vaatverwijdende respons en andere aspecten van endotheelfunctie werd verwacht dat de resultaten wat groter zouden zijn geweest [2].
De studie geeft geen mechanistisch inzicht in de vraag waarom dalcetrapib de endotheelfunctie niet verbeterde, ondanks een significante verhoging van HDL-C niveaus. Inclusie van patiënten met normale HDL-C niveaus op baseline kan het moeilijk hebben gemaakt om een verbetering laten zien, maar subgroep-analyse bij patiënten met een laag HDL-C liet ook geen enkele verbetering van de endotheelfunctie zien.
CETP modulatie door dalcetrapib zou HDL kunnen genereren dat functioneel inactief is, althans voor wat betreft endotheelfunctie, waardoor er verdere vraagtekens zijn te plaatsen bij de controverse over CETP als een legitiem therapeutisch doelwit voor atherosclerose [3].
Reactiviteit van de arteria brachialis is slechts een surrogaat van vasculaire gezondheid. Interventies die de reactiviteit verbeteren, geven niet perse een verbetering van de klinische uitkomsten; gebrek aan verbetering in de reactiviteit van de arteria brachialis sluit niet noodzakelijk klinisch voordeel uit. De onlangs gerapporteerde resultaten van dalcetrapib op imagingresultaten van atherosclerose in de dal-PLAQUE studie zijn enigszins bemoedigend [4].
Ondanks de negatieve (endotheelfunctie, inflammatoire markers) of marginaal positieve effecten op surrogaat eindpunten (plaque), kunnen alleen grootschalige event-based klinische studies uiteindelijk beoordelen of CETP remming met specifieke remmers zonder de off-target toxische effecten van torcetrapib therapeutisch gunstig zal zijn. De resultaten van de dal-OUTCOMES studie zullen beschikbaar komen in 2013 en hopelijk meer informatie geven over de rol van CETP in atherosclerose. Surrogaatmarkers houden geen rekening met andere bekende of onbekende biologische vasculaire en niet-vasculaire effecten die uiteindelijk van invloed zijn op de netto klinische resultaten. Laten we wachten op de resultaten!
 | ESC: Inzichten in lipiden/atheroscleroseProf. J.W. Jukema, cardioloog, LUMC, Leiden geeft een update over het laatste nieuws zoals gepresenteerd tijdens de ESC op het gebied van lipiden en atherosclerose. (6:12 min). De volgende geselecteerde onderwerpen worden besproken zijn ASCOT-LLA, dal-VESSEL en CORP. |
Referenties
1. Shah PK. Cholesteryl ester transfer protein inhibition and endothelial function: enough with the surrogates Eur Heart J 2012 published 20 February 2012, 10.1093/eurheartj/ehs040
2. Chyu KY, Peter A, Shah PK. Progress in HDL-based therapies for atherosclerosis. Curr Atheroscler Rep 2011;13:405–412
3. Shah PK. The yin and yang of cholesteryl ester transfer protein in cardiovascular disease. Circulation 2009;120:2408–2410.
4. Fayad ZA, Mani V, Woodward M, Kallend D, Abt M, Burgess T, Fuster V, Ballantyne CM, Stein EA, Tardif JC, Rudd JH, Farkouh ME, Tawakol A; dal-PLAQUE Investigators. Safety and efficacy of dalcetrapib on atherosclerotic disease using novel non-invasive multimodality imaging (dal-PLAQUE): a randomized clinical trial. Lancet 2011;378:1547–1559
Abstract
Aims High-density lipoprotein cholesterol (HDL-C) is inversely associated with cardiovascular (CV) events and thus an attractive therapeutic target. However, in spite of marked elevations in HDL-C, the first cholesterol transport protein (CETP) inhibitor torcetrapib raised blood pressure (BP), impaired endothelial function, and increased CV mortality and morbidity. Dalcetrapib is a novel molecule acting on CETP with a different chemical structure to torcetrapib. As HDL stimulates nitric oxide (NO), suppresses inflammation, and exerts protective CV effects, we investigated the effects of dalcetrapib on endothelial function, blood pressure, inflammatory markers, and lipids in patients with, or at risk of, coronary heart disease (CHD) in a double-blind randomized placebo-controlled trial (clinicaltrials.gov number NCT00655538).
Conclusion The dal-VESSEL trial has established the tolerability and safety of CETP-inhibition with dalcetrapib in patients with or at risk of CHD. Dalcetrapib reduced CETP activity and increased HDL-C levels without affecting NO-dependent endothelial function, blood pressure, or markers of inflammation and oxidative stress. The dal-OUTCOMES trial (NCT00658515) will show whether dalcetrapib improves outcomes in spite of a lack of effect on endothelial function.

Deel deze pagina met collega's en vrienden: