Darmflora-afhankelijke metabolietniveaus hebben prognostische waarde in hartfalen
Literatuur - Tang et al., J Am Coll Cardiol. 2014
Prognostic Value of Elevated Levels of Intestinal Microbe-Generated Metabolite Trimethylamine-N-Oxide in Patients With Heart Failure Refining the Gut Hypothesis
Tang WHW, Wang Z, Fan Y et al.,
J Am Coll Cardiol. 2014;64(18):1908-1914. doi:10.1016/j.jacc.2014.02.617
Achtergrond
De bijdrage van het gastrointestinale system aan de pathogenese van hartfalen (HF) wordt steeds meer erkend [1,2]. Een evenwichtige intestinale microbioom onderhoudt normaalgesproken de intestinale barrièrefunctie, alsmede de mucosale immuniteit en normale zout- en waterhuishouding. In HF en geassocieerde splanchnische circulatiecongestie, kunnen veranderde intestinale barrièrefunctie, bacteriële wildgroei en verstoorde afweer van de gastheer de bacteriële omgeving verstoren. Uiteindelijk kan dit leiden tot systemische inflammatie [3,4]. Progressieve veneuze congestie in sommige patiënten kan daarbij abdominale congestie verergeren, inclusief het negatief beïnvloeden van medicijnabsorptie en farmacokinetiek [5,6], en renale glomerulaire en tubulaire dysfunctie als gevolg van verhoogde intra-abdominale druk [7,8].Een mechanistische link is eerder beschreven tussen intestinale microbe-afhankelijke productie van trimethylamine-N-oxide (TMAO) en verhoogd risico op toekomstige cardiovasculaire events, via een signaalroute waarvoor voedingsstoffen als phosphatidylcholine, choline (gevonden in eieren) en carnitine (in rood vlees) gebruikt worden [9-11]. De auteurs onderzochten de relatie tussen nuchtere plasma TMAO niveaus en lange termijn (5 jaar) klinische prognose in patiënten met HF.
Belangrijkste resultaten
- Gemiddeld TMAO niveau in het HF cohort was 5.0 µM (IQR: 3.0-8.5 µM), in vergelijking met 3.5 µM (IQR: 2.3-5.7) in het gezonde cohort (P<0.001).
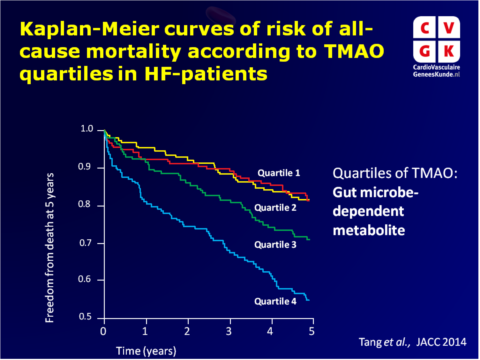
- Kaplan-Meier analyse van TMAO-gestratificeerde kwartielen laat een geleidelijke stijging van het sterfterisico zien, met name wanneer TMAO niveaus hoger zijn dan mediane levels. Binnen het HF cohort, werd hoge sterfte gezien in het 4e TMAO kwartiel in vergelijking met het 1e kwartiel (HR: 3.42, 95%CI: 2.24-5.23, P<0.001).
- Mortalieit risico’s geassocieerd met TMAO niveaus waren vergelijkbaar in ischaemische en niet-ischaemische patiënten met HF.
- Toevoeging van TMAO aan een risicopredictiemodel met traditionele CV risicofactoren verbeterde de netto herclassificering significant (integrated discrimination improvement: 16.0%, P<0.001, net reclassification index: 10.9%, P<0.001).
- Een significant maar bescheiden correlatie werd gezien tussen TMAO en BNP niveaus (r-0.23, P<0.001). De correlatie tussen TMAO en eGFR was sterker (r= -0.55, P<0.001).
- Zelfs in een model dat corrigeerde voor traditionele risicofactoren, BNP, eGRF en hsCRP, bleken hoge TMAO niveaus geassocieerd met verhoogde mortaliteit (HR: 1.85, 95%CI: 1.14-3.00, P<0.05).
Conclusie
Deze studie laat zien dat plasma TMAO niveaus een sterke prognostische waarde hebben in patiënten met stabiel hartfalen, in aanvulling op traditionele risicofactoren, cardiorenale indexen (BNP en eGFR) en een marker voor systemische inflammatie (hsCRP). Deze observaties specificeren de ‘darm hypothese’, namelijk dat darmflora de prognose beïnvloeden bij patiënten met HF. Studies zijn nodig die verkennen of gerichte interventies om de samenstelling van de darmflora te veranderen TMAO niveaus kunnen verlagen, en daarmee ziekteprogressie van HF kunnen beperken.Redactioneel commentaar [12]
“De sterke correlatie tussen TMAO concentratie en nierfunctie roept de volgende vraag op: gezien het belang van de nier in het uitscheiden van TMAO, is een hogere TMAO niveau slechts een marker van nierstoornis? Andere vragen zijn, bijvoorbeeld ook wat de rol van co-morbiditeiten zijn, zoals diabetes, in het verhogen van TMAO niveaus? Diabetes kwam aanzienlijk vaker voor in de hogere TMAO groep, en van metformine is gerapporteerd dat het TMAO niveaus verhoogt (en intestinale microben spelen mogelijk een rol in de ontwikkeling van diabetes). Verwarrender is nog hoe TMAO zelf gerelateerd kan zijn aan prognose. Het is onwaarschijnlijk dat een proatherogeen mechanisme een verhoogde mortaliteit kan verklaren in zo’n kort tijdsbestek, met name in patiënten met niet-obstructief coronairlijden. (…) Het is duidelijk dat dit slechts het begin is van het verhaal van TMAO in HF, en we moeten uitzien naar verdere afleveringen.”Vind dit artikel online
Referenties
1. Krack A, Sharma R, Figulla HR, Anker SD. The importance of the gastrointestinal system in thepathogenesis of heart failure. Eur Heart J 2005; 26:2368–74.
2. Verbrugge FH, Dupont M, Steels P, et al. Abdominal contributions to cardiorenal dysfunction
in congestive heart failure. J Am Coll Cardiol 2013;62:485–95.
3. Rauchhaus M, Anker SD. Plasma concentrations of bacterial lipopolysaccharide: a marker of
infection or inflammation? J Am Coll Cardiol 2000;36:656–7.
4. Sandek A, Bauditz J, Swidsinski A, et al. Altered intestinal function in patients with chronic heart
failure. J Am Coll Cardiol 2007;50:1561–9.
5. Vasko MR, Cartwright DB, Knochel JP, et al. Furosemide absorption altered in decompensated congestive heart failure. Ann Intern Med 1985;102:314–8.
6. Carlton LD, Pollack GM, Brouwer KL. Physiologic pharmacokinetic modeling of gastrointestinal
blood flow as a rate-limiting step in the oral absorption of digoxin: implications for patients with congestive heart failure receiving epoprostenol. J Pharm Sci 1996;85:473–7.
7. Mullens W, Abrahams Z, Skouri HN, et al. Elevated intra-abdominal pressure in acute decompensated heart failure: a potential contributor to worsening renal function? J Am Coll Cardiol
2008;51:300–6.
8. Mullens W, Abrahams Z, Francis GS, et al. Importance of venous congestion for worsening of renal function in advanced decompensated heart failure. J Am Coll Cardiol 2009;53: 589–96.
9. Wang Z, Klipfell E, Bennett BJ, et al. Gut flora metabolism of phosphatidylcholine promotes
cardiovascular disease. Nature 2011;472:57–63.
10. Tang WH, Wang Z, Levison BS, et al. Intestinal microbial metabolism of phosphatidylcholine and
cardiovascular risk. N Engl J Med 2013;368: 1575–84.
11. Koeth RA, Wang Z, Levison BS, et al. Intestinal microbiota metabolism of l-carnitine, a nutrient
in red meat, promotes atherosclerosis. Nat Med 2013;19:576–85.
12. Cannon JA, McMurray JJV. Gut feelings about heart failure. J Am Coll Cardiol 2014;64;18:1915-1916

Deel deze pagina met collega's en vrienden: