Renale denervatie geeft duurzame bloeddrukverlaging tot ten minste 36 maanden
Literatuur - Esler MD et al., Eur Heart J. 2014 - Eur Heart J. 2014 Jul 7;35(26):1752-9
Catheter-based renal denervation for treatment of patients with treatment-resistant hypertension: 36 month results from the SYMPLICITY HTN-2 randomized clinical trial
Esler MD, Böhm M, Sievert H, et al.
Eur Heart J. 2014 Jul 7;35(26):1752-9
Achtergrond
Patiënten met behandel-resistente hypertensie (bloeddruk (BP) >140/90 mmHg ondanks >3 antihypertensieve middelen, inclusief een diureticum), hebben vaak ook andere cardiovasculaire (CV) risicofactoren, waardoor zij een nog hoger risico lopen op eindorgaan schade en CV morbiditeit [1]. Schattingen van echt behandel-resistente hypertensie lopen uiteen van 5 tot 16% [2-6].Renale sympathische outflow is vaak overactief bij patiënten met essentiële hypertensie. In experimentele diermodellen werd voor het eerst aangetoond dat het chirurgisch doorsnijden van de nierzenuw BP verlaagt [7,8].
Bij percutane cathetergebaseerde renale denervatie (RDN) wordt laag-vermogen (~8W) radiofrequente energie bij de grootste nierarterie toegediend, in een spiraalpatroon van ablaties [9,10]. De SYMPLICITY HTN-1 proof-of-principle studie toonde de haalbaarheid van de procedure aan, en patiënten met ernstige behandelresistente hypertensie hadden een duurzame BP-daling voor ten minste 3 jaar [11-13].
De SYMPLICITY HTN-2 was een gerandomiseerde klinische trial die de veiligheid en effectiviteit van RND met medisch management vergeleek met alleen medisch management (controlegroep) in patiënten met ernstige behandelresistente hypertensie [14.15]. Een significante daling vanaf baseline BP werd gezien 6 maanden na randomisatie naar RDN (-32/-12 mmHG, P<0.0001), terwijl geen significante verandering in BP werd gezien in de controlegroep. De SYMPLICITY HTN-2 studie gaf deelnemers in de controlegroep de gelegenheid tot crossover om RDN te krijgen na de initiële 6-maanden primaire eindpunt evaluatie. Deze publicatie rapporteert de 36 maanden follow-up van de initiële RDN–groep (n=40) en 30 maanden follow-up van de crossover deelnemers die 6 maanden later RDN kregen (n=30).
Belangrijkste resultaten
- Baseline SBP was 178+18 mmHg in de RDN groep en 191+20 mmHg in de crossover groep.
- SBP en DBP metingen waren significant lager dan de pre-procedurele metingen, op alle tijdspunten (6, 12, 24, 30 en 36 maanden). Daline van BP verminderde niet tijdens follow-up. Na 30 maanden was de daling van SBP -34 mmHg (95%CI: -40 tot -27, P<0.01) en verandering van DBP was -13 mmHg (95%CI: -16 tot -10, P<0.01). Daling van BP was vergelijkbaar voor de originele RDN en de crossover patiënten.
- Respons rate van het bereiken van een SBP daling van > 20 mmHg was vergelijkbaar voor de originele RDN deelnemers (72%) en crossover deelnemers (70%).
- Hartslag was lager na RDN, en de daling duurde voort tot 36 maanden (gemiddelde daling 4 bpm (95%CI: -8 to -0.1, P=0.04).
- Na 30 maanden was het gemiddeld aantal antihypertensiva gedaald van 5.1+1.4 bij baseline tot 4.8+1.5 (P=0.06) middelen.
- Complicaties geassocieerd met de procedure betroffen één haematoom, en één renale arteriedissectie voor energietoediening, welke met succes kon worden behandeld. Tussen 12 en 36 maanden na de procedure, traden 5 hypertensieve events op die ziekenhuisopname behoefden, en een geval van mild voorbijgaand acuut nierfalen werd gerapporteerd. Drie sterfgevallen werden gezien tijdens follow-up, welke werden beschouwd als niet gerelateerd aan de device of de behandeling.
Download Esler EHJ 2014 CVGK.pptx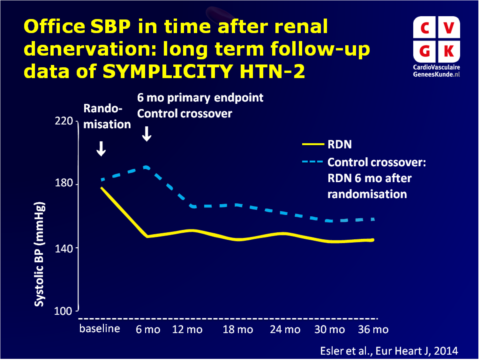
Conclusie
Deze publicatie voegt langetermijngegevens toe aan de veiligheid en effectiviteit van RDN, door de duurzaamheid van de antihypertensieve effecten van RDN zoals gezien in de eerdere SYMPLICITY HTN-1 studie te bevestigen, in patiënten met ernstige behandelresistente hypertensie. Het langetermijneffect werd behaald zonder dat medicatie werd uitgebreid, en zonder ernstige lange termijn veiligheidsissues.Deze gegevens komen niet overeen met de korter durende SYMPLICITY HTN-3 studie, waarin geen significant verschil werd gezien tussen RDN en een nepprocedure. De beter getrainde operatoren in de deelnemende centra in SYMPLICITY HTN-2 kunnen dit verschil mogelijk deels verklaren.
Klik door naar dit artikel op Pubmed
Referenties
1. Calhoun DA, Jones D, Textor S, et al., American Heart Association Professional Education C. Resistant hypertension: diagnosis, evaluation, and treatment: a scientific statement from the American Heart Association Professional Education Committee of the Council for High Blood Pressure Research. Circulation 2008;117:e510–e526.
2. Sarafidis PA, Bakris GL. Resistant hypertension: an overview of evaluation and treatment. J Am Coll Cardiol 2008;52:1749–1757.
3. Wojciechowski D, Papademetriou V, Faselis C, Fletcher R. Evaluation and treatment of resistant or difficult-to-control hypertension. J Clin Hypertens (Greenwich) 2008;10: 837–843.
4. Daugherty SL, Powers JD, Magid DJ, et al. Incidence and prognosis of resistant hypertension in hypertensive patients. Circulation 2012;125:1635–1642.
5. Persell SD. Prevalence of resistant hypertension in the United States, 2003–2008. Hypertension 2011;57:1076–1080.
6. de la Sierra A, Segura J, Banegas JR, et al. Clinical features of 8295 patients with resistant hypertension classified on the basis of ambulatory blood pressure monitoring. Hypertension 2011;57: 898–902.
7. DiBona GF, Esler M. Translational medicine: the antihypertensive effect of renal denervation. Am J Physiol Regul Integr Comp Physiol 2010;298:R245–R253.
8. Foss JD, Fink GD, Osborn JW. Reversal of genetic salt-sensitive hypertension by targeted sympathetic ablation. Hypertension 2013;61:806–811.
9. Atherton DS, Deep NL, Mendelsohn FO. Micro-anatomy of the renal sympathetic nervous system: a human postmortem histologic study. Clin Anat 2012;25:628–633.
10. Johns EJ, Kopp UC, DiBona GF. Neural control of renal function. Compr Physiol 2011; 1:731–767.
11. Krum H, Schlaich M, Whitbourn R, et al. Catheter-based renal sympathetic denervation for resistant hypertension: a multicentre safety and proof-of-principle cohort study. Lancet 2009;373:1275–1281.
12. Symplicity HTNI. Catheter-based renal sympathetic denervation for resistant hypertension: durability of blood pressure reduction out to 24 months. Hypertension 2011; 57:911–917.
13. Krum H, Schlaich MP, Sobotka PA, et al. Percutaneous renal denervation in patients with treatment-resistant hypertension: final 3-year report of the Symplicity HTN-1 study. Lancet 2014;383: 622–629.
14. Esler MD, Krum H, Sobotka PA, et al. Renal sympathetic denervation in patients with treatment-resistant hypertension (The Symplicity HTN-2 Trial): a randomised controlled trial. Lancet 2010;376:1903–1909.
15. Esler MD, Krum H, Schlaich M, et al. Symplicity HTNI. Renal sympathetic denervation for treatment of drug-resistant hypertension: one-year results from the Symplicity HTN-2 randomized, controlled trial. Circulation 2012;126:2976–2982.

Deel deze pagina met collega's en vrienden: